Cho hỗn hợp gồm Cu và Fe 2 O 3 (với tỉ lệ mol 1 : 1) tác dụng với dung dịch HCl dư. Lấy dung dịch thu được cho tác dụng với NH 3 dư, thu được kết tủa là
A. Fe OH 3
B. Cu OH 2 và Fe OH 3
C. Fe OH 2
D. Cu OH 2
Hỗn hợp X gồm Cu, Ag, Fe2O3 có tỉ lệ số mol tương ứng là 1:2:1. Cho 44 gam hỗn hợp X tác dụng với dung dịch HCl dư, thu được chất rắn Y và dung dịch Z. Cho dung dịch Z tác dụng với dung dịch NaOH dư (không có không khí) đến khi phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là
A. 27,8.
B. 24,1.
C. 21,4.
D. 28,7.
Hỗn hợp X gồm Cu, Ag, Fe2O3 có tỉ lệ số mol tương ứng là 1:2:1. Cho 44 gam hỗn hợp X tác dụng với dung dịch HCl dư thu được chất rắn Y và dung dịch Z. Cho dung dịch Z tác dụng với dung dịch NaOH dư (không có không khí) đến khi phản ứng xảy ra hoàn toàn thu được m gam kết tủa. Giá trị của m là
A. 27,8 gam
B. 24,1 gam
C. 21,4 gam
D. 28,7 gam
Đáp án : A
Trong 44g X có : nCu = 0,1 ; nAg = 0,2 ; nFe2O3 = 0,1 mol
X + HCl -> Z( CuCl2 ; FeCl2) + NaOH dư (không có không khí) -> Fe(OH)2 ; Cu(OH)2
=> Kết tủa gồm : 0,1 mol Cu(OH)2 và 0,2 mol Fe(OH)2
=> m = 27,8g
Hỗn hợp X gồm Fe3O4 và Cu (tỉ lệ mol là 1:2). Cho m gam X tác dụng vừa đủ với dung dịch chứa 0,08 mol HCl, kết thúc phản ứng thu được dung dịch Y và còn lại m1 gam chất rắn Z. Cho dung dịch Y tác dụng với dung dịch AgNO3 dư thu được m2 gam kết tủa. Giá trị của m1, m2 lần lượt là
A. 0,64 và 11,48 gam
B. 0,64 và 3,24 gam.
C. 0,64 và 14,72 gam
D. 0,32 và 14,72 gam.
Hỗn hợp X gồm F e 3 O 4 và Cu (tỉ lệ mol là 1: 2). Cho m gam X tác dụng vừa đủ với dung dịch chứa 0,08 mol HCl, kết thúc phản ứng thu được dung dịch Y và còn lại m1 gam chất rắn Z. Cho dung dịch Y tác dụng với dung dịch A g N O 3 (dư) thu được m2 gam kết tủa. Giá trị của m1, m2 lần lượt là
A. 0,64 và 14,72
B. 0,64 và 3,24
C. 0,32 và 14,72
D. 0,64 và 11,48
Đáp án A
Kết thúc phản ứng còn dư lại m1 (g) chất rắn Z
=> Z là Cu, dd Y gồm FeCl2 và CuCl2.
Fe3O4 + 8HCl → 2FeCl3 + FeCl2
0,01<---- 0,08 ------> 0,01
=> n C u = 0,02
2FeCl3 + Cu → 2FeCl2 + CuCl2
0,02 -----> 0,01 --> 0,02
=> n C u dư = 0,01 => m1 = 6,4g
dd Y tác dụng với A g N O 3
Ag+ + Cl- → AgCl
0,08 <--- 0,08 ----> 0,08
Fe2+ + Ag+ → Fe3+ + Ag
0,03 → 0,03
=> m2 = 0,03.108 + 0,08.143,5 = 14,72g
Hỗn hợp X gồm Fe2O3 và Cu. Cho m gam hỗn hợp X tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 122,76 gam chất tan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 loãng vừa đủ thu được dung dịch Y chứa 3 chất tan với tỉ lệ số mol 1 : 2 : 3. Dung dịch Y làm mất màu tối đa bao nhiêu gam KMnO4 trong môi trường axit sunfuric?
A. 6,162
B. 6,004.
C. 5,846.
D. 5,688
Chọn đáp án D
Xét thí nghiệm 2: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4 → n C u S O 4 : n F e S O 4 = 1 : 2 .
⇒ n C u S O 4 : n F e S O 4 : n F e 2 ( S O 4 ) 3 = 1 : 2 : 3 .
Đặt n C u S O 4 = x mol ⇒ n F e S O 4 = 2x mol và n F e 2 ( S O 4 ) 3 = 3x mol.
⇒ n C u 2 + = x mol; n F e 2 + = 2x mol; n F e 3 + = 6x mol
⇒ n C u C l 2 = x mol; n F e C l 2 = 2x mol; n F e C l 3 = 6x mol.
⇒ mchất tan = 135x + 127 × 2x + 162,5 × 6x = 122,76 gam ⇒ x = 0,09 mol.
⇒ Y chứa 0,18 mol FeSO4. Bảo toàn electron: 5 n K M n O 4 = n F e S O 4 .
![]()
![]()
Hỗn hợp X gồm Fe2O3 và Cu. Cho m gam hỗn hợp X tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 122,76 gam chất tan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 loãng vừa đủ thu được dung dịch Y chứa 3 chất tan với tỉ lệ số mol 1 : 2 : 3. Dung dịch Y làm mất màu tối đa bao nhiêu gam KMnO4 trong môi trường axit sunfuric?
A. 6,162.
B. 6,004.
C. 5,846.
D. 5,688.
Xét thí nghiệm 2: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O.
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
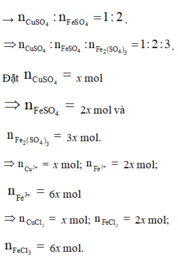
mchất tan = 135x + 127 × 2x + 162,5 × 6x = 122,76 gam ⇒ x = 0,09 mol.
Y chứa 0,18 mol FeSO4. Bảo toàn electron:
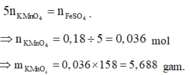
Đáp án D
Cho 1,37g hỗn hợp X gồm Fe và kim loại M hoá trị không đổi tác dụng với dung dịch HCl dư thấy giải phóng 1,232 lít khí H2 (đkc). Mặt khác hỗn hợp X trên tác dụng vừa đủ với lượng khí Cl2 điều chế được bằng cách cho 3,792 gam KMnO4 tác dụng với dung dịch HCl đặc dư. Tỉ lệ số mol của Fe và M trong hỗn hợp là 1: 3. Kim loại M là
A. Mg
B. Cu
C. Al
D. Zn
Đáp án : C
X + HCl : Fe -> Fe2+ có nH2 = 0,055 mol
X + Cl2 : Fe -> Fe3+
bảo toàn e : 5nKMnO4 = 2nCl2 => nCl2 = 0,06 mol
Do M có hóa trị không đổi => nFe = ne (2) – ne (1) = 2nCl2 – 2nH2 = 0,01 mol
Giả sử M có hóa trị n => n.nM + 2.0,01 = 2nH2 => n.nM = 0,09 mol
Có : mX = 1,37g = 0,01.56 + nM.M => nM.M = 0,81g
=> M = 9n
Nếu n = 3 => M = 27g (Al) Thỏa mãn
Cho các thí nghiệm sau:
(a) Cho Ba(OH)2 dư tác dụng với dung dịch Al2(SO4)3.
(b) Cho Na2CO3 tác dụng với dung dịch FeCl3.
(c) Cho hỗn hợp Cu, Fe3O4 (tỉ lệ mol 1:1) vào lượng dư dung dịch HCl.
(d) Cho Mg vào lượng dư dung dịch Fe2(SO4)3.
(e) Cho hỗn hợp gồm Ba, Al (tỉ lệ mol 1:3) vào lượng dư H2O.
(f) Cho một mẩu gang vào lượng dư dung dịch H2SO4 loãng.
(g) Cho dung dịch NaHCO3 vào dung dịch Ba(OH)2 (dư).
Sau khi các phản ứng xảy ra hoàn toàn. Số thí nghiệm thu được chất rắn sau phản ứng là
A. 6.
B. 4.
C. 3.
D. 5.
Chọn D.
(a) Chất rắn thu được là BaSO4.
(b) Chất rắn thu được là Fe(OH)3.
(c) Phản ứng vừa đủ thu được dung dịch có chứa hai muối và axit dư.
(d) Dung dịch thu được chứa ba muối tan.
(e) Chất rắn thu được là Al dư.
(f) Chất rắn không tan trong H2SO4 loãng là C.
(g) Chất rắn thu được là BaCO3.
Hỗn hợp X gồm Fe2O3 và Cu. Cho m gam hỗn hơp X tác dụng với dung dịch HCl vừa đủ thu được dung dịch chứa 122,76 gam chất tan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 loãng vừa đủ thu được dung dịch Y chứa 3 chất tan với tỉ lệ số mol 1 : 2 : 3. Dung dịch Y làm mất màu tối đa bao nhiêu gam KMnO4 trong môi trường axit sunfuric?
A. 6,162
B. 5,846
C. 5,688
D. 6,004